ข้อสอบ PAT
วันอาทิตย์ที่ 8 กันยายน พ.ศ. 2562
การใช้ประโยชน์ของสารประกอบไอออนิก สารโคเวเลนต์ และโลหะ
จากการที่สารประกอบไอออนิกสารโคเวเลนต์และโลหะมีสมบัติเฉพาะตัวมาว่าการที่ต่างกันจึงสามารถนำมาใช้ประโยชน์ในด้านต่างๆได้ตามความเหมาะสม เช่น
- แอมโมเนียมคลอไรด์และซิงค์คลอไรด์ เป็นสารประกอบไอออนิกที่สามารถนำไฟฟ้าได้จากการแตกตัวเป็นไอออนเมื่อละลายน้ำจึงนำไปใช้เป็นสารอิเล็กโทรไลต์ในถ่านไฟฉาย
- พอลิไวนิลคลอไรด์หรือ PVC เป็นสารโคเวเลนต์ที่ไม่สามารถนำไฟฟ้าได้จึงเป็นฉนวนไฟฟ้าที่หุ้มสายไฟฟ้า
- ซิลิกอนคาร์ไบด์ เป็นสารโคเวเลนต์โครงร่างตาข่ายที่มีจุดหลอมเหลวสูงและมีความแข็งแรงมากจึงนำไปใช้ทำเครื่องบด
- ทองแดงและอะลูมิเนียม เป็นโลหะที่นําไฟฟ้าได้ดีจึงนำไปใช้เป็นตัวนำไฟฟ้าอลูมิเนียมและเหล็กเป็นโลหะที่นําความร้อนได้ดีจึงนำไปทำภาชนะสำหรับประกอบอาหาร เช่น หม้อ กระทะ
วันเสาร์ที่ 7 กันยายน พ.ศ. 2562
พันธะโลหะ
การเกิดพันธะโลหะ
การที่อะตอมโลหะมีค่าพลังงานไอออไนเซชันต่ำ การยึดเหนี่ยวระหว่างเวเลนซ์อิเล็กตรอนกับโปรตอนในนิวเคลียสจึงน้อย ทำให้เวเลนซ์อิเล็กตรอนสามารถเคลื่อนที่ได้อย่างอิสระไปทั่วทั้งชิ้นโลหะและเกิดการยึดเหนี่ยวกับโปรตอนในนิวเคลียสทุกทิศทาง เรียกว่า พันธะโลหะ แสดงได้ด้วยแบบจำลองทะเลอิเล็กตรอน
สมบัติของโลหะ
พันธะโลหะ (Metallic Bond) คือ แรงดึงดูดระหว่างไอออนบวกซึ่งเรียงชิดกันกับอิเล็กตรอนที่อยู่โดยรอบหรือเป็นแรงยึดเหนี่ยวที่เกิดจากอะตอมในก้อนโลหะใช้เวเลนซ์อิเล็กตรอนทั้งหมดร่วมกัน
การเกิดพันธะโลหะ
การที่อะตอมโลหะมีค่าพลังงานไอออไนเซชันต่ำ การยึดเหนี่ยวระหว่างเวเลนซ์อิเล็กตรอนกับโปรตอนในนิวเคลียสจึงน้อย ทำให้เวเลนซ์อิเล็กตรอนสามารถเคลื่อนที่ได้อย่างอิสระไปทั่วทั้งชิ้นโลหะและเกิดการยึดเหนี่ยวกับโปรตอนในนิวเคลียสทุกทิศทาง เรียกว่า พันธะโลหะ แสดงได้ด้วยแบบจำลองทะเลอิเล็กตรอน
สมบัติของโลหะ
พันธะโลหะ (Metallic Bond) คือ แรงดึงดูดระหว่างไอออนบวกซึ่งเรียงชิดกันกับอิเล็กตรอนที่อยู่โดยรอบหรือเป็นแรงยึดเหนี่ยวที่เกิดจากอะตอมในก้อนโลหะใช้เวเลนซ์อิเล็กตรอนทั้งหมดร่วมกัน
พันธะโลหะจะมีความสำคัญต่อคุณสมบัติทางฟิสิกส์หลายอย่างของโลหะเช่น
- ความแข็งแรง
- ตีแผ่เป็นแผ่นได้
- ดึงเป็นเส้นได้
- นำความร้อนไดดี
- นำไฟฟ้าได้ดีและนำได้ทุกทิศทาง
- เนื้อเป็นเงา
พันธะโคเวเลนต์
การเกิดพันธะโคเวเลนต์
พันธะเคมีที่เกิดขึ้นระหว่างอะตอมของธาตุอโลหะกับธาตุโลหะที่เข้ามาสร้างแรงยึดเหนี่ยวต่อกัน เนื่องจากธาตุอโลหะจะมีสมบัติเป็นตัวรับอิเล็กตรอนที่ดีและยากต่อการสูญเสียอิเล็กตรอน ดังนั้นอิเล็กตรอนของธาตุทั้งสองจึงต่างส่งแรงดึงดูดเพื่อที่จะดึงดูดอิเล็กตรอนของอีกฝ่ายให้เข้าหาตนเอง ทำให้แรงดึงดูดจากนิวเคลียสของอะตอมทั้งสองหักล้างกัน
ตารางเเสดงความยาวพันธะ
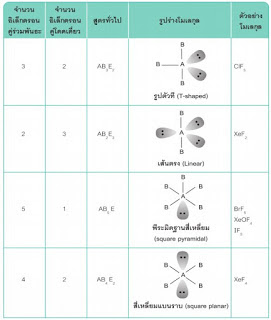
รูปร่างโมเลกุลโคเวเลนต์
สภาพของขั้วของโมเลกุล
ถ้ามีการกระจายของกลุ่มหมอกอิเล็กตรอนคู่ร่วมพันธะระหว่างอตอมทั้งสองเท่ากัน เรียกว่า พันธะโคเวเลนต์ไม่มีขั้ว ส่วนสารโคดวดลนต์ที่เกิดจากอะตอมต่างชนิดกันและมีค่าอิเล็กโทรเนกาติวิตีต่างกันจะมีการกระจายตัวของกลุ่มหมอกอิเล็กตรอนคู่ร่วมพันธะระหว่างอะตอมไม่เท่ากัน เรียกว่า พันธะโคเวเลนต์มีขั้ว
การเกิดพันธะโคเวเลนต์
พันธะเคมีที่เกิดขึ้นระหว่างอะตอมของธาตุอโลหะกับธาตุโลหะที่เข้ามาสร้างแรงยึดเหนี่ยวต่อกัน เนื่องจากธาตุอโลหะจะมีสมบัติเป็นตัวรับอิเล็กตรอนที่ดีและยากต่อการสูญเสียอิเล็กตรอน ดังนั้นอิเล็กตรอนของธาตุทั้งสองจึงต่างส่งแรงดึงดูดเพื่อที่จะดึงดูดอิเล็กตรอนของอีกฝ่ายให้เข้าหาตนเอง ทำให้แรงดึงดูดจากนิวเคลียสของอะตอมทั้งสองหักล้างกัน
พันธะเดี่ยว (single bond) คือ พันธะโคเวเลนต์ที่เกิดจากอะตอมคู่ที่เข้ามาร่วมสร้างพันธะต่อกันมีการใช้ร่วมสร้างพันธะต่อกันมีการใช้อิเล็กตรอนร่วมกัน 1 คู่
พันธะคู่ (double bond) คือ พันธะโคเวเลนต์ที่เกิดจากอะตอมคู่ที่เข้ามาร่วมสร้างพันธะต่อกันมีการใช้อิเล็กตรอนร่วมกัน 2 คู่
พันธะสาม (triple bond) คือ พันธะโคเวเลนต์ที่เกิดจากอะตอมคู่ที่เข้ามาร่วมสร้างพันธะต่อกัน มีการใช้อิเล็กตรอนร่วมกัน 3 คู่
สูตรโมเลกุลและชื่อของสารโคเวเลนต์
การอ่านชื่อสารโคเวเลนต์ มีวิธีการอ่านดังนี้
- อ่านจำนวนอะตอมพร้อมชื่อธาตุแรก (ในกรณีธาตุแรกมีอะตอมเดียวไม่ต้องอ่านจำนวน )
- อ่านจำนวนอะตอม และชื่อธาตุที่สอง ลงท้ายเป็น ไ-ด์ (ide )
เลขจำนวนอะตอมอ่านเป็นภาษากรีก คือ
1 = mono 2 = di
3 = tri 4 = tetra
5 = penta 6 = hexa
7 = hepta 8 = octa
9 = nona 10 = deca
ความยาวพันธะและพลังงานพันธะของสารโคเวเลนต์
ตารางเเสดงพลังงาน
ถ้ามีการกระจายของกลุ่มหมอกอิเล็กตรอนคู่ร่วมพันธะระหว่างอตอมทั้งสองเท่ากัน เรียกว่า พันธะโคเวเลนต์ไม่มีขั้ว ส่วนสารโคดวดลนต์ที่เกิดจากอะตอมต่างชนิดกันและมีค่าอิเล็กโทรเนกาติวิตีต่างกันจะมีการกระจายตัวของกลุ่มหมอกอิเล็กตรอนคู่ร่วมพันธะระหว่างอะตอมไม่เท่ากัน เรียกว่า พันธะโคเวเลนต์มีขั้ว
แรงยึดเหนี่ยวระหว่างโมเลกุลและสมบัติของสารโคเวเลนต์
แรงลอนดอน เป็นแรงยึดเหนี่ยวระหว่างโมเลกุล ยึดเหนี่ยวกันด้วยแรงอ่อนๆ ซึ่งเกิดขึ้นในสารทั่วไป และจะมีค่าเพิ่มขึ้นตามมวลโมเลกุลของสาร
แรงดึงดูดระหว่างขั้ว เป็นแรงดึงดูดทางไฟฟ้าอันเนื่องมาจากแรงกระทำระหว่างขั้วบวกกับขั้วลบของโมเลกุลที่มีขั้ว
พันธะไฮโดรเจน คือ แรงดึงดูดระหว่างโมเลกุลที่เกิดจากไฮโดรเจนอะตอมสร้างพันธะโคเวเลนต์ กับอะตอมที่มีค่าอิเล็กโทรเนกาติวิตีสูงๆและมีขนาดเล็ก ได้แก่ F , O และ N แล้วเกิดพันธะโคเวเลนต์มีขั้วชนิดมีสภาพขั้วแรงมาก และอะตอมของธาตุที่มีค่าอิเล็กโทรเนกาติวิตีสูง ยังมีอิเล็กตรอนคู่โดดเดี่ยว จึงเกิดดึงดูดกันระหว่างอิเล็กตรอนคู่โดดเดี่ยวกับอะตอมของไฮโดรเจน
ซึ่งมีอำนาจไฟฟ้าบวกสูงของอีกโมเลกุลหนึ่ง ทำให้เกิดเป็นพันธะไฮโดรเจน
สารโคเวเลนต์โครงร่างตาข่าย
สารโคเวเลนต์ที่ศึกษามาแล้วมีโครงสร้างโมเลกุลขนาดเล็ก มีจุดหลอมเหลวและจุดเดือดต่ำ แต่มีสารโคเวเลนต์บางชนิดมีโครงสร้างโมเลกุลขนาดยักษ์ มีจุดหลอมเหลวและจุดเดือดสูงมาก เนื่องจากอะตอมสร้างพันธะโคเวเลนต์ยึดเหนี่ยวกันทั้งสามมิติเกิดเป็นโครงสร้างคล้ายตาข่ายสารประเภทนี้เรียกว่าสารโครงผลึกร่างตาข่ายตัวอย่างสารโครงผลึกร่างตาข่าย
ซึ่งมีอำนาจไฟฟ้าบวกสูงของอีกโมเลกุลหนึ่ง ทำให้เกิดเป็นพันธะไฮโดรเจน
สารโคเวเลนต์โครงร่างตาข่าย
สารโคเวเลนต์ที่ศึกษามาแล้วมีโครงสร้างโมเลกุลขนาดเล็ก มีจุดหลอมเหลวและจุดเดือดต่ำ แต่มีสารโคเวเลนต์บางชนิดมีโครงสร้างโมเลกุลขนาดยักษ์ มีจุดหลอมเหลวและจุดเดือดสูงมาก เนื่องจากอะตอมสร้างพันธะโคเวเลนต์ยึดเหนี่ยวกันทั้งสามมิติเกิดเป็นโครงสร้างคล้ายตาข่ายสารประเภทนี้เรียกว่าสารโครงผลึกร่างตาข่ายตัวอย่างสารโครงผลึกร่างตาข่าย
พันธะไอออนิก
การเกิดพันธะไอออนิก
พันธะไอออนิก เป็นพันธะเคมีชนิดหนึ่ง เกิดจากที่อะตอมหรือกลุ่มของอะตอมสร้างพันธะกันโดยที่อะตอมหรือกลุ่มของอะตอมให้อิเล็กตรอนกับอะตอมหรือกลุ่มของอะตอม ทำให้กลายเป็นประจุบวก ในขณะที่อะตอมหรือกลุ่มของอะตอมที่ได้รับอิเล็กตรอนนั้นกลายเป็นประจุลบ เนื่องจากทั้งสองกลุ่มมีประจุตรงกันข้ามกันจะดึงดูดกัน ทำให้เกิดพันธะไอออน โดยทั่วไปพันธะชนิดนี้มักเกิดขึ้นระหว่างโลหะกับอโลหะ
การเกิดพันธะไอออนิก
พันธะไอออนิก เป็นพันธะเคมีชนิดหนึ่ง เกิดจากที่อะตอมหรือกลุ่มของอะตอมสร้างพันธะกันโดยที่อะตอมหรือกลุ่มของอะตอมให้อิเล็กตรอนกับอะตอมหรือกลุ่มของอะตอม ทำให้กลายเป็นประจุบวก ในขณะที่อะตอมหรือกลุ่มของอะตอมที่ได้รับอิเล็กตรอนนั้นกลายเป็นประจุลบ เนื่องจากทั้งสองกลุ่มมีประจุตรงกันข้ามกันจะดึงดูดกัน ทำให้เกิดพันธะไอออน โดยทั่วไปพันธะชนิดนี้มักเกิดขึ้นระหว่างโลหะกับอโลหะ
สูตรเคมีและชื่อของสารประกอบไอออนิก
พลังงานกับการเกิดสารประกอบไอออนิก
พลังงานที่เกี่ยวข้องกับการรวมกันของไอออนบวกและลบในสารประกอบไอออนิกเรียกว่า พลังงานโครงผลึก สามารถหาค่าพลังงานได้ด้วยการคำนวณ โดยอาศัยวัฏจักรบอร์น-ฮาเบอร์ ประกอบด้วยขั้นตอนต่างๆดังนี้
1.ของแข็งระเหิดกลายเป็นแก๊ส เรียกพลังงานที่ใช้ในขั้นนี้ว่า พลังงานการระเหิด
2.พลังงานที่ใช้ในการเสียอิเล็กตรอนให้กลายเป็นไอออนบวกเป็นไอออนลบ เรียกว่า พลังงานไอออไนเซชัน
3.พลังงานที่ใช้ในการสลายโมเลกุลของแก๊สให้เป็นอะตอมในสถานะแก๊ส เรียก พลังงานการสลายพันธะ
4.พลังงานที่คายออกมาเมื่อมีการรับอิเล็กตรอนให้กลายเป็นประจุลบเรียกว่า พลังงานสัมพรรรคภาพอิเล็กตรอน5.
พลังงานที่ได้ออกมาเมื่อมีการยึดไอออนบวกกับไอออนลบให้กลายเป็นของแข็ง เรียกว่า พลังงานโครงผลึกหรือพลังงานแลตทิซ
สมบัติของสารประกอบไอออนิก
1.มีขั้ว สารประกอบไอออนิกไม่ได้เกิดขึ้นเป็นโมเลกุลเดี่ยว แต่จะเป็นของแข็งซึ่งประกอบด้วยไอออนจำนวนมากซึ่งยึดเหนี่ยวกัน ด้วยแรงยึดเหนี่ยวทางไฟฟ้า
2.นำไฟฟ้าได้ เมื่อใส่สารประกอบไอออนนิกลงในน้ำ ไอออนจะแยกออกจากัน ทำให้สารละลายนำไฟฟ้าได้
3.มีจุดหลอมเหลวและจุดเดือดสูง เพราะต้องการพลังงานความร้อนในการทำลายแรงดึงดูดระหว่างไอออนให้กลายเป็นของเหลว
4.การละลาย สารประกอบไอออนิกจะละลายในน้ำแต่ไม่ละลายในเบนซีนหรือตัวทำละลายอินทรีย์ น้ำและตัวทำละลายชนิดมีขั้ว
5.สารประกอบไอออนิกทำให้เกิดปฏิกริยาไอออนิก คือ ปฏิกริยาระหว่างไอออนกับไอออน ทั้งนี้เพราะสารไอออนิกจะเป็นไอออนอิสระในสารละลาย ปฎิกริยาจึงเกิดทันที
6.เป้นผลึกเเข็งเเต่เปราะง่าย
สมการไอออนิกเเละสมการไอออนิกสุทธิ
สมการไอออนิกสุทธิ (net ionic equation) จะเป็นสมการที่เขียนเฉพาะไอออนที่ทำปฏิกิริยากันได้เป็นผลิตภัณฑ์เท่านั้น โดยผลรวมประจุทางซ้ายและทางขวาของสมการต้องดุลกันพอดี เช่น
การผสมสารละลายซิลเวอร์ไนเตรต (AgNO3) และโซเดียมคลอไรด์ (NaCl) ได้ตะกอนสีขาวของซิลเวอร์คลอไรด์ (AgCl) ซึ่งไม่ละลายน้ำ
สามารถเขียนสมการทั่วไป สมการไอออนิกและสมการไอออนิกสุทธิได้
การทำนายปฏิกิริยาการเกิดตะกอนของสารละลายของสารประกอบไอออนิก สามารถพิจารณาได้จากสมบัติการละลายน้ำ ดังนี้
สารประกอบที่ละลายน้ำ
- สารประกอบของโลหะแอลคาไลน์และแอมโมเนียมทุกชนิด
- สารประกอบไนเทรต คลอเรต เปอร์คลอเรต แอซีเตต
- สารประกอบคลอไรด์ โบรไมด์ ไอโอไดด์ ยกเว้นสารประกอบของ Ag+ Pb2+ Hg2+ ไม่ละลาย ส่วน PbCl2 ละลายได้น้อย
- สารประกอบซัลเฟต (ยกเว้นสารประกอบของ Pb2+ Sr2+ Ba2+ ส่วนสารประกอบของ Ca2+ และ Ag+ ละลายได้น้อย)
สารประกอบที่ไม่ละลายน้ำ
- สารประกอบของออกไซด์ของโลหะ (ยกเว้นออกไซด์ของ Ca2+ Sr2+ Ba2+)
- สารประกอบไฮดรอกไซด์ (ยกเว้นไฮดรอกไซด์ของโลหะแอลคาไล แอมโมเนียมและของ Sr2+ Ba2+ ส่วนของCa2+ ละลายได้น้อย)
- สารประกอบคาร์บอเนต ฟอสเฟต ซัลไฟด์และซัลไฟต์ (ยกเว้นสารประกอบของโลหะแอลคาไล)
สัญลักษณ์แบบจุดของลิวอิสและกฎออกเตต
สูตรโครงสร้างของลิวอิส
เป็นสูตรโครงสร้างที่กิลเบิร์ต ลิวอิสได้คิดค้นขึ้นมาเพื่อใช้ในการอธิบายรูปร่างโมเลกุล ซึ่งจะแบ่งได้เป็น 2 ประเภทได้แก่
-สูตรโครงสร้างส่วนที่เป็นจุด เป็นสูตรโครงสร้างที่ใช้จุดแทนอิเล็กตรอนวงนอกสุดของอะตอมที่เกิดพันธะ โดยให้อิเล็กตรอนครบตามกฎออกเตต ยกเว้นบางธาตุซึ่งมีการยกเว้นได้
-สูตรโครงสร้างส่วนที่เป็นเส้น เป็นสูตรโครงสร้างที่ใช้เส้นและจุดแทนอิเล็กตรอนวงนอกสุดของอะตอมที่เกิดพันธะ ซึ่งเส้น 1 เส้นจะแทนอิเล็กตรอน 2 ตัวหรือ 1 คู่ สามารถเขียนอิเล็กตรอนเดี่ยวด้วยก็ได้
กฎออกเตต
ธาตุก๊าซเฉื่อย เช่น He Ne Ar Kr พบว่าเป็นธาตุที่โมเลกุลเป็นอะตอมเดี่ยว คือในหนึ่งโมเลกุลของก๊าซเฉื่อยจะมีเพียง 1 อะตอม แสดงว่าเป็นธาตุที่เสถียรมาก ทำให้นักวิทยาศาสตร์สนใจที่จะค้นคว้าถึงเหตุผลที่ทำให้ธาตุเฉื่อยมีความเสถียร และจากการศึกษาโครงสร้างอะตอมของธาตุเฉื่อยมีการจัดเรียงอิเล็กตรอนวงนอกสุดเหมือนกัน คือมี 8 อิเล็กตรอน(ยกเว้น He มี 2 อิเล็กตรอน) เช่น
2He = 2 10Ne = 2 , 8 18Ar = 2 , 8 , 8 36Kr = 2 , 8 , 18 , 8
ส่วนธาตุหมู่อื่นมีการจัดเรียงอิเล็กตรอนในระดับพลังงานชั้นนอกสุด ไม่ครบ 8 เช่น
ธาตุที่มีวาเลนต์อิเล็กตรอนไม่ครบ 8 ในธรรมชาติจะไม่สามารถอยู่เป็นอะตอมเดี่ยวๆได้ ซึ่งแสดงว่าไม่เสถียร การรวมกันเพื่อทำให้อะตอม มีวาเลนต์อิเล็กตรอนครบ 81H = 1 6C = 2 , 4 7N = 2 , 5 8O = 2 , 6
การนำธาตุไปใช้ประโยชน์เเละผลกระทบต่อสิ่งมีชีวิต
ประโยชน์ของธาตุ
-ธาตุโลหะ นำความร้อนและนำไฟฟ้าได้ดี นิยมนำมาทำเป็นอุปกรณ์ไฟฟ้า
-ธาตุกึ่งโลหะ มีสมบัติก้ำกึ่งระหว่างโลหะและอโลหะ นำไฟฟ้าได้ไม่ดี นิยมนำมาทำเป็นสารกึ่งตัวนำ ซึ่งมีสมบัติในการนำไฟฟ้าอยู่ระหว่างตัวนำและฉนวนเพื่อใช้เป็นวัสดุทำอุปกรณ์อิเล็กทรอนิกส์ต่างๆ
-ธาตุหมู่ 18 หรือ VIIA เป็นธาตุเฉื่อยต่อการเกิดปฏิกิริยาจึงนำมาใช้ประโยชน์ตามสมบัติของแก๊สมีสกุล
-ธาตุที่มีไอโซโทปกัมมันตรังสี สามารถนำมาใช้ประโยชน์ได้หลากหลายดังที่กล่าวไปในหัวข้อ 2.6.6 แม้ธาตุอยู่ในกลุ่มเดียวกันจะมีสมบัติคล้ายกัน แต่ธาตุทุกชนิดยังมีสมบัติต่างกัน ดังนั้นการนำไปใช้ประโยชน์จึงมีความจำเพาะต่างกัน
ผลกระทบต่อสิ่งมีชีวิตและสิ่งแวดล้อม
1.ถ้าร่างกายได้รับจะทำให้โมเลกุลภายในเซลล์เกิดการเปลี่ยนแปลงไม่สามารถทำงานตามปกติได้ ถ้าเป็นเซลล์ที่เกี่ยวข้องกับการถ่ายทอดลักษณะพันธุกรรมก็จะเกิดการผ่าเหล่า โดยเฉพาะเซลล์สืบพันธุ์เมื่อเข้าไปในร่างกายจะไปสะสมในกระดูก
2. ส่วนผลที่ทำให้เกิดความป่วยไข้จากรังสี เมื่ออวัยวะส่วนใดส่วนหนึ่งของร่างกายได้รับรังสี โมเลกุลของธาตุต่างๆ ที่ประกอบเป็นเซลล์จะแตกตัว ทำให้เกิดอาการป่วยไข้และเกิดมะเร็งได้
ธาตุกัมมันตรังสี
การเกิดธาตุกัมมันตรังสี
นิวเคลียสของธาตุกัมมันตรังสีมีพลังงานสูงมากและไม่เสถียร จึงปล่อยพลังงานออกมาในรูปของอนุภาคหรือรังสีบางชนิด แล้วธาตุเหล่านั้นก็จะเปลี่ยนเป็นธาตุใหม่ ต่อมารัทเทอร์ฟอร์ดได้ศึกษาเพิ่มเติมและแสดงให้เห็นว่ารังสีที่แผ่ออกมาจากธาตุกัมมันตรังสีอาจเป็นรังสีแอลฟา บีตาหรือแกมมา ที่มีสมบัติแตกต่างกัน
การสลายตัวของไอโซโทปกัมมันตรังสี
การแผ่รังสีแอลฟา ส่วนใหญ่เกิดกับนิวเคลียสที่มีเลขอะตอมสูงกว่า 83 และมีจำนวนนิวตรอนต่อโปรตอนในจำนวนที่ไม่เหมาะสม
การเกิดธาตุกัมมันตรังสี
นิวเคลียสของธาตุกัมมันตรังสีมีพลังงานสูงมากและไม่เสถียร จึงปล่อยพลังงานออกมาในรูปของอนุภาคหรือรังสีบางชนิด แล้วธาตุเหล่านั้นก็จะเปลี่ยนเป็นธาตุใหม่ ต่อมารัทเทอร์ฟอร์ดได้ศึกษาเพิ่มเติมและแสดงให้เห็นว่ารังสีที่แผ่ออกมาจากธาตุกัมมันตรังสีอาจเป็นรังสีแอลฟา บีตาหรือแกมมา ที่มีสมบัติแตกต่างกัน
การสลายตัวของไอโซโทปกัมมันตรังสี
การแผ่รังสีแอลฟา ส่วนใหญ่เกิดกับนิวเคลียสที่มีเลขอะตอมสูงกว่า 83 และมีจำนวนนิวตรอนต่อโปรตอนในจำนวนที่ไม่เหมาะสม
การแผ่รังสีบีตา เกิดกับนิวเคลียสที่มีจำนวนนิวตรอนมากกว่าโปรตอนมาก นิวตรอนในนิวเคลียสจะเปลี่ยนไปเป็นโปรตอนและอิเล็กตรอน โดยจะออกมาในรูปของรังสีบีตาและนิวเคลียสใหม่จะมีเลขอะตอมเพิ่มมาอีก 1 โดยที่เลขมวลยังเท่าเดิม
การแผ่รังสีแกมมา เกิดกับไอโซโทปกัมมันตรังสีที่มีพลังงานสูงมาก หรือไอโซโทปที่สลายตัวให้รังสีแอลฟาหรือบีตา แต่นิวเคลียสที่เกิดใหม่ยังไม่เสถียรเพราะมีพลังงานสูงจึงเกิดการเปลี่ยนแปลงในนิวเคลียสให้มีพลังงานต่ำลงโดยปล่อยออกมาในรูปรังสีแกมมา
อันตรายจากไอโซโทปกัมมันตรังสี
โดยธรรมชาติแล้วมีธาตุที่แผ่รังสีออกมาเองได้ประมาณ 60 ชนิด เป็นรังสีที่เราพบได้ในแต่ละวัน แต่มันมีปริมาณน้อยหรือไม่ก็ไม่ส่งผลอันตรายต่อร่างกายของเรา กลุ่มนี้เรียกว่า กัมมันตภาพรังสีจากพื้นโลก อีกส่วนคือส่วนที่มาจากนอกโลกซึ่งเรียกว่า กัมมันตภาพจากรังสีคอสมิกซึ่งบางส่วนก็หลุดลอดชั้นบรรยากาศของโลกเข้ามาได้ และอีกส่วนเกิดขึ้นจากน้ำมือมนุษย์ กิจกรรมต่าง ๆ อุปกรณ์และเครื่องมือต่างๆ เช่น การใช้รังสีเอ็กซ์ในทางการแพทย์ การตรวจสอบความปลอดภัย หรือการใช้กัมมันตภาพรังสีในการถนอมอาหารในโรงงานอุตสาหกรรมเป็นต้น
ครึ่งชีวิตของไอโซโทปกัมมันตรังสี
ครึ่งชีวิตของไอโซโทปกัมมันตรังสี
ครึ่งชีวิต ใช้สัญลักษณ์ t1/2 หมายถึง ระยะเวลาที่นิวเคลียสของไอโซโทปกัมมันตรังสีสลายตัวจนเหลือครึ่งนึของปริมาณเดิม
ปฎิกิริยานิวเคลียร์
ปฏิกิริยานิวเคลียร์ในธรรมชาติจะเกิดขึ้นจากการปฏิสัมพันธ์ระหว่างรังสีคอสมิกและสสาร และปฏิกิริยานิวเคลียร์สามารถถูกประดิษฐ์ขึ้นเพื่อให้ได้พลังงานนิวเคลียร์ในอัตราที่ปรับได้ตามความต้องการ บางทีปฏิกิริยานิวเคลียร์ที่โดดเด่นมากที่สุดจะเป็นปฏิกิริยาลูกโซ่นิวเคลียร์ในวัสดุที่แตกตัวได้ เพื่อเหนี่ยวนำให้เกิดปฏิกิริยานิวเคลียร์ฟิชชั่นและปฏิกิริยานิวเคลียร์ฟิวชันต่างๆขององค์ประกอบเบาที่ผลิตพลังงานให้กับดวงอาทิตย์และดวงดาวทั้งหลาย ทั้งสองประเภทในการเกิดปฏิกิริยานี้ถูกใช้ในการผลิตอาวุธนิวเคลียร์
เทคโนโลยีที่เกี่ยวข้องกับการใช้สารกัมมันตรังสี
ด้านธรณีวิทยา ใช้คาร์บอน - 14 ซึ่งมีครึ่งชีวิต 5,730 ปี หาอายุของวัตถุโบราณที่มีคาร์บอนเป็นองค์ประกอบเช่น ไม้ กระดูก หรือสารอินทรีย์อื่น ๆ การหาอายุวัตถุโบราณโดยการวัดปริมาณของ คาร์บอน – 14 ซึ่งเกิดจากไนโตรเจนรวมตัวกับนิวตรอน
ด้านการแพทย์ ใช้เพื่อศึกษาความผิดปกติของอวัยวะต่าง ๆ ในร่างกาย โดยให้คนไข้รับประทานอาหารหรือยาที่มีไอโซโทปกัมมันตรังสีจำนวนเล็กน้อย จากนั้นใช้เครื่องมือตรวจสอบรังสีเพื่อติดตามดูผลการดูดซึมไอโซโทปกัมมันตรังสีของระบบอวัยวะต่าง ๆ
ด้านเกษตรกรรม ใช้ไอโซโทปกัมมันตรังสีในการติดตามระยะเวลาของการหมุนเวียนแร่ธาตุในพืช โดยเริ่มต้น จากการดูดซึมที่รากจนถึงการคายออกที่ใบหรือจำนวนแร่ธาตุที่พืชสะสมไว้ที่ใบ
ด้านอุตสาหกรรม ใช้ไอโซโทปกัมมันตรังสีกับงานหลายอย่าง เช่น ใช้ตรวจหารอยตำหนิในโลหะหรือรอยรั่วของท่อขนส่งของเหลว ในอุตสาหกรรมการทำอัญมณีใช้รังสีเพื่อทำให้อัญมณีมีสีสันสวยงามขึ้น โดยใช้รังสีแกมมา นิวตรอน หรืออิเล็กตรอนพลังงานสูงฉายไปบนอัญมณี จะทำให้สารที่ทำให้เกิดสีบนอัญมณีเปลี่ยนสีไปได้
อัญมณีที่ฉายด้วยรังสีแกมมาจะไม่มีรังสีตกค้างแต่การอาบด้วยนิวตรอนจะมีไอโซโทปกัมมันตรังสีเกิดขึ้น จึง
ต้องปล่อยให้ไอโซโทปกัมมันตรังสีสลายตัวจนมีระดับที่ปลอดภัยจึงนำมาใช้ประโยชน์
ธาตุเเทรนซิชัน
ธาตุแทรนซิชัน คือ กลุ่มธาตุที่อยู่ระหว่างหมู่ IIA กับ IIIA ซึ่งก็คือธาตุหมู่ B ทั้งหมด ประกอบด้วยหมู่ IB – VIIIB รวมทั้ง อินเนอร์แทรนซิชัน ได้แก่ กลุ่มแลนทาไนด์ และกลุ่มแอกทิไนด
ธาตุแทรนซิชัน เป็นธาตุที่ใช้อิเล็กตรอนในระดับพลังงานย่อย ในการเกิดพันธะ ยกเว้นธาตุหมู่ 2B ที่ใช้อิเล็กตรอนในระดับพลังงานย่อย s ในการเกิดพันธะ
ธาตุแทรนซิชันในคาบที่ 4 ได้แก่ Sc , Ti , V , Cr , Mn , Fe , Co , Ni , Cu , Zn
สมบัติของธาตุเเทรนซิชัน
ธาตุทรานซิชันเป็นโลหะทุกธาตุ แต่ไม่ได้อยู่กลุ่มเดียวกับธาตุหมู่ IIA และ IIIA
1.รัศมีอะตอมมีขนาดใกล้เคียงกัน
2.สารประกอบส่วนมากมีสี
3.เป็นโลหะที่มีจุดหลอมเหลว จุดเดือดสูง
4.เป็นตัวนำไฟฟ้าและตัวนำความร้อนที่ดี
ธาตุแทรนซิชัน คือ กลุ่มธาตุที่อยู่ระหว่างหมู่ IIA กับ IIIA ซึ่งก็คือธาตุหมู่ B ทั้งหมด ประกอบด้วยหมู่ IB – VIIIB รวมทั้ง อินเนอร์แทรนซิชัน ได้แก่ กลุ่มแลนทาไนด์ และกลุ่มแอกทิไนด
ธาตุแทรนซิชัน เป็นธาตุที่ใช้อิเล็กตรอนในระดับพลังงานย่อย ในการเกิดพันธะ ยกเว้นธาตุหมู่ 2B ที่ใช้อิเล็กตรอนในระดับพลังงานย่อย s ในการเกิดพันธะ
ธาตุแทรนซิชันในคาบที่ 4 ได้แก่ Sc , Ti , V , Cr , Mn , Fe , Co , Ni , Cu , Zn
สมบัติของธาตุเเทรนซิชัน
ธาตุทรานซิชันเป็นโลหะทุกธาตุ แต่ไม่ได้อยู่กลุ่มเดียวกับธาตุหมู่ IIA และ IIIA
1.รัศมีอะตอมมีขนาดใกล้เคียงกัน
2.สารประกอบส่วนมากมีสี
3.เป็นโลหะที่มีจุดหลอมเหลว จุดเดือดสูง
4.เป็นตัวนำไฟฟ้าและตัวนำความร้อนที่ดี
ตารางธาตุและสมบัติของธาตุหมู่หลัก
วิวัฒนาการของการสร้างตารางธาตุ
ปี พ.ศ. 2360 (ค.ศ. 1817) โยฮันน์ โวล์ฟกัง เดอเบอไรเนอร์ พยายามจัดธาตุเป็นกลุ่มๆละ 3 ธาตุตามสมบัติที่คล้ายคลึงกันเรียกว่า ชุดสาม
พ.ศ. 2407 (ค.ศ. 1864) จอห์น นิวแลนด์ เสนอกฎการจัดธาตุเป็นหมวดหมู่ เรียงธาตุตามมวลอะตอมจากน้อยไปมาก พบว่าธาตุที่ 8 จะมีสมบัติเหมือนกับธาตุที่ 1 เสมอ ตารางธาตุมีวิวัฒนาการมาเรื่อยๆจนถึงปัจจุบันนี้
ยูลิอุสโยทาร์ ไมเออร์ นักวิทยาศาสตร์ชาวเยอรมัน และเดมิทริ อิวาโนวิช เมเดเลเอฟ นักวิทยาศาสตร์ชาวรัสเซีย ได้ศึกษารายละเอียดของธาตุมากขึ้น พบว่าถ้าจัดเรียงธาตุตามมวลอะตอมจากน้อยไปหามาก ธาตุจะมีสมบัติคล้ายกันเป็นช่วง ๆ เมเดเลเอฟจึงตั้งเป็นกฎเรียกว่า “กฎพีริออดิก” โดยได้เสนอความคิดนี้ในปี พ.ศ. 2412 ก่อนที่ไมเออร์จะเสนอผลงานเพียงหนึ่งปี เพื่อเป็นเกียรติแก่เมเดเลเอฟ จึงเรียกตารางนี้ว่า ตารางพีริออดิกของเมเดเลเอฟ
กลุ่มของธาตุในตารางธาตุ
แบ่งได้เป็น 3 กลุ่ม คือ ธาตุโลหะ ธาตุกึ่งโลหะ และธาตุอโลหะ โดยธาตุโลหะจะอยู่ทางซ้ายมือของตารางธาตุ ธาตุกึ่งโลหะจะอยู่บริเวณที่เป็นขั้นบันได และธาตุอโลหะจะอยู่ทางขวามือของตารางธาตุ ยกเว้นไฮโดรเจนที่อยู่ทางซ้ายมือของตาราง
ขนาดอะตอม
จากการศึกษาโครงสร้างอะตอมตามทฤษฎีของโบร์ (Bohr Theory) อิเล็กตรอนในอะตอมจะมีระดับพลังงานได้หลายค่า และเมื่ออิเล็กตรอนอยู่ห่างนิวเคลียสมากก็จะยิ่งมีพลังงานสูง ดังนั้นขนาดของอะตอมจะเล็กหรือใหญ่จึงขึ้นอยู่กับอิเล็กตรอนในชั้นนอกสุดว่าอยู่ในระดับพลังงานใด และขึ้นอยู่กับจำนวนโปรตอนในนิวเคลียส ซึ่งจะมีความสัมพันธ์กับหมู่และคาบของธาตุในตารางธาตุด้วย
ขนาดไอออน
| อะตอมซึ่งมีจำนวนโปรตอนเท่ากับอิเล็กตรอน เมื่ออะตอมรับอิเล็กตรอนเพิ่มเข้ามาหรือเสียอิเล็กตรอนออกไป อะตอมจะเปลี่ยนไปเป็นไอออนเมื่อโลหะทำปฏิกิริยากับอโลหะ อะตอมของโลหะจะเสียเวเลนซ์อิเล็กตรอนกลายเป็นไอออนบวก จำนวนอิเล็กตรอนในอะตอมจึงลดลง ทำให้แรงผลักระหว่างอิเล็กตรอนลดลงด้วย พลังงานไอออไนเซชัน พลังงานไอออไนเซชัน คือ พลังงานที่ให้แก่อะตอม เพื่อให้อะตอมในสถานะแก๊สกลายเป็นไอออนบวกและยังเป็นการดึงอิเล็กตรอนออกจากอะตอมนั้นด้วย
Li(g)
- ธาตุที่มีอิเล็กตรอน 1 ตัว คือ ธาตุไฮโดรเจน(H)
H(g)
พลังงานปริมาณน้อยที่สุดที่ทำให้อิเล็กตรอนหลุดจากอะตอมในสถานะแก๊สเรียกว่า พลังงานไอออไนเซชัน (IE) โดยค่า IE แสดงถึงความยากง่ายในการทำให้อะตอมในสถานะแก๊สกลายเป็นไอออนบวกโดย IE มากแสดงว่าทำให้เป็นไอออนบวกได้ยาก ถ้าเป็นธาตุที่มีหลายอิเล็กตรอนก็จะมีพลังงานไอออไนเซชันหลายค่า พลังงานน้อยที่สุดที่ทำให้อิเล็กตรอนตัวแรกหลุดออกมาจากอะตอมที่อยู่ในสถานะแก๊สเรียกว่า พลังงานไอออไนเซชันลำดับที่หนึ่ง สัมพรรคภาพอิเล็กตรอน
พลังงานที่ถูกคายออกมาเมื่ออะตอมในสถานะแก๊สได้รับอิเล็กตรอน 1 อิเล็กตรอน เรียกว่า สัมพรรคภาพอิเล็กตรอน (EA) ถ้าค่า EA เป็นบวก หมายความว่าอะตอมคายพลังงานเมื่อได้รับอิเล็กตรอน แสดงว่าอะตอมของธาตุนั้นมีแนวโน้มที่จะรับอิเล็กตรอนได้ดี
อิเล็กโทรเนกาติวิตีอิเล็กโทรเนกาติวิตี (electronegativity : EN) หมายถึงค่าที่แสดงความสามารถในการดึงดูดอิเล็กตรอนของอะตอมคู่ที่เกิดพันธะที่จะรวมกันเป็นโมเลกุล ธาตุที่มีค่าอิเล็กโทรเนกาติวิตีสูงตะมีความสามารถในการดึงดูดหรือรับอิเล็กตรอนได้ดี ได้แก่พวกอโลหะ ส่วนธาตุที่มีค่าอิเล็กโทรเนกาติวิตีต่ำจะดึงดูดหรือรับอิเล็กตรอนได้ไม่ดี ได้แก่พวกโลหะ เช่น โมเลกุลของ HCl เนื่องจาก Cl ดึงดูดอิเล็กตรอนได้ดีกว่า H ดังนั้น Cl จึงมีค่าอิเล็กโทรเนเติวิตีสูงกว่า H |
สมัครสมาชิก:
ความคิดเห็น (Atom)